
ページ読込中...

ページ読込中...

[English]
| 石渡 信一 [教授] |  |
|
| homepage | https://www.phys.waseda.ac.jp/wps/bio/ishiwata | |
| 専門分野 | 生物物理学 | |
| 研究テーマ・研究活動 | ||
| ○生体分子モーターの動作メカニズム ○筋収縮系の自励振動メカニズム ○筋収縮系・細胞骨格系の構造と機能の再構築 ○細胞分裂機構の力学操作・解析 ○超分子システムにおける1分子機能・分子間協調 |
||
| ●日本生物物理学会会長(2004-2005年度 ●日本物理学会 ●日本生化学会 ●日本生理学会 ●アメリカ生物物理学会 |
||
| 編著: 「生体分子モーターの仕組み」(共立)、 「ナノピコスペースのイメージング」(吉岡書店)、 「実験生物物理」(丸善) | ||
生物は、分子から個体に至る階層構造をなしています。タンパク質分子とその集合体、それらが細胞膜に取り囲まれた細胞、何種類もの細胞が集まった細胞集団、そして心臓だとか肝臓だとかの特殊な生体機能を備えた臓器や器官が作り上げられ、それらが組み合わさって生物個体が出来上がっています。私たちは常日頃、生物個体を見て、その生物は生きているとか、死んでいると言いますが、では、どの階層で生死の境が決まるのでしょうか。 また、生物が生きていくために、どの階層で“生物らしさ”が生まれているのでしょうか。 私たちは、生物のあらゆる階層に見られる運動性(生体運動)に注目しています。生体運動は、筋収縮運動に限らず、植物細胞に見られる原形質流動、卵分割や細胞分裂、白血球などのアメーバ運動、それに神経細胞内部の軸索輸送など、細胞が形を変える運動から、細胞内部の物質輸送や、細胞膜を介する能動輸送にかかわる運動など、実に多種多様です。
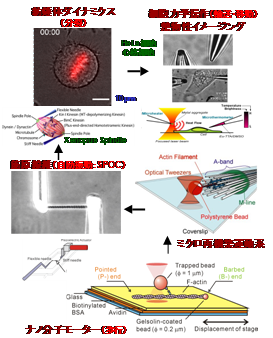
ところが、このように見かけは違いますが、生体運動を担っているタンパク質には共通性があることが分かってきました。化学エネルギーを力学エネルギーに変換するタンパク質分子機械(大きさが10nm程度)、これを総称して“生体分子モーター”と呼びます。 筋収縮運動は2つの足を持ったミオシン分子モーターの集団とアクチンフィラメントとの相互作用によって生まれますし、神経細胞内部の軸索輸送は、微小管の上を1分子のキネシン分子モーターが2つの足を交互に動かすことによって行われることが分かりつつあります。 物理学科の中にあって、“生物物理学”という学問分野を開拓しようとしている私たちは、“生体分子モーター”を研究対象にして、“生物らしい仕組みとはどのようなものか”という問いに答えるべく、物理学的研究手法や見方・考え方をよりどころにしつつ、日夜研究を続けています。
| Shin’ichi Ishiwata [Professor] |  |
|
| homepage | https://www.phys.waseda.ac.jp/wps/bio/ishiwata | |
| research field | Solving the mechanism of biological functions – From single molecule to systems | |
| research keywords | ||
| Hierarchical organization in bio-motile systems Molecular motors as auto-oscillators Nano- and micro-mechanics of molecular motors, myofibrils, and meiotic spindles |
||
| link | ||
Biological functions are inherently hierarchical. For many years we have been studying the underlying mechanisms of biological functions from the single-molecule level to the level of supramolecular assemblies, focusing on mechanisms which are characteristic of each level of the hierarchy. We have clarified, in particular, the existence of mechanochemical coupling (intramolecular synchronization) between the intramolecular load and enzymatic activity during the movement of single molecular motors such as kinesin and myosin V (VI) on cytoskeletons (microtubules and actin filaments). In our laboratory, we have been focusing on intracellular movement, auto-oscillation of the contractile systems of muscles, and cell division (chromosome segregation) as typical examples of biological movement, trying to make clear whether the forces produced by the molecular motors and cytoskeleton play an important role in the regulation of the elementary processes of motion such as transport, oscillation, and division. That is, we intend to show that the chemo-mechanical feedback loop (CMF loop:) exists throughout the whole hierarchical organization, possessing, however, different mechanisms characteristic of each level. Through this approach, we try to demonstrate that the CMF loop mechanism is a common principle for the regulation of biomotility. We also aim to develop a technique that will allow the use of the cytoskeleton as a “bionanogauge” that will allow, for example, the monitoring of stress imposed on the cytoskeleton. Furthermore, we examine the role of other physical parameters such as heat and temperature.On the single-molecule level, we examine the role of the CMF loop in the mechanisms of the motility and depolymerization/severing of cytoskeletal tracks by measuring rupture force and determining the binding mode of various myosins and regulating proteins with actin, as well as kinesins (such as MCAK) with microtubules. In myofibrils we focus on the molecular mechanism of the auto-oscillation (SPOC), especially in cardiac muscle, coupled with the construction of the theoretical model. Concerning cell division, we concentrate on the balance of tension in the mechanisms of chromosome segregation, perturbing it by applying external forces to the mitotic cells. This approach will allow us to confirm the existence of the CMF loop and make clear its mechanisms on various levels of biological hierarchy.
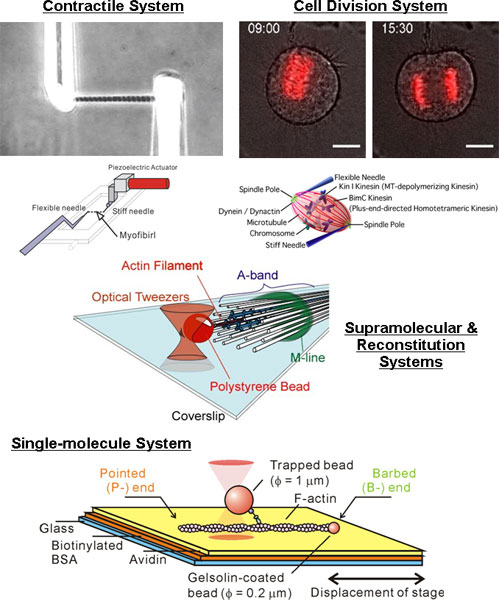
Our research objective is to show clearly, on the molecular level, the existence of the CMF loop throughout the hierarchy of bio-motile systems, from single molecules and ensembles to supramolecular organizations, cells, and tissues. This will clarify the (common regulatory) mechanism of biological motility and will possibly become a prime achievement of biophysical research.